
 1,166 Views
1,166 Viewsในภาวะที่มีภูมิคุ้มกันเสื่อมโดยไวรัสไปทำลาย CD4+T cells หรือที่เรียกชื่อเดิมว่า T helper ลดลงไปอย่างมากจนกระทั่งทำให้เกิดโรคเอดส์เต็มขั้นนั้น การรักษาจะต้องดำเนินไปดังต่อไปนี้
๑. การบริบาลทั่วไปและการรักษาประคับประคอง อันได้แก่ การดูแลผู้ป่วยโดยทั่วไปและการให้อาหาร ให้พลังงานสารน้ำอิเล็กโทรไลต์ ฯลฯ ให้พอเพียงและให้การรักษาทางจิตบำบัด เป็นต้น
๒. การรักษาตามอาการ เช่น การรักษาอาการไข้ อาการท้องเดิน เป็นต้น
๓. การรักษาเฉพาะโรคที่เกิดขึ้น ได้แก่ รักษาโรคติดเชื้อฉวยโอกาส เช่น การรักษาโรคปอดบวม โรคติดเชื้อแคนดิดา โรคระบบประสาทและรักษาโรคมะเร็ง โดยการฉายรังสีหรือเคมีบำบัด เป็นต้น
๔. การให้ยาต้านเชื้อไวรัสเอชไอวีเพื่อระงับยับยั้งการทวีจำนวนของไวรัสในเซลล์ชนิดต่าง ๆ
๕. การให้ยากระตุ้นการทำงานของระบบภูมิคุ้มกันเพื่อให้มีการสร้างหรือเสริมปรับปรุงระบบภูมิคุ้มกันที่เสียไปให้ฟื้นกลับมาใหม่ แม้ว่าจะไม่ดีขึ้นเท่าเดิมก็ดีกว่าปล่อยให้ภูมิคุ้มกันเสื่อมอย่างเต็มที่
ในที่นี้จะได้กล่าวถึงสารที่มีฤทธิ์ระงับยับยั้งมิให้ไวรัสทวีจำนวนในเซลล์และสารปรับปรุงระบบอิมมูน (Immune Modulator) ในปัจจุบันกล่าวได้ว่ายังไม่มียาหรือสารต้านไวรัสชนิดใดที่ทรงประสิทธิภาพสูงหรือที่เรียกว่า เป็นยา "อุดมคติ" ส่วนใหญ่จะมีฤทธิ์เพียงแต่ยับยั้งการเจริญเพิ่มจำนวนของไวรัสเท่านั้น
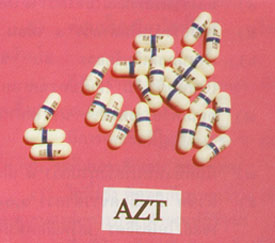
๑.๑ ยาที่มีฤทธิ์ยับยั้งเอนไซม์รีเวอร์สทรานสคริพเตสที่มีใช้อยู่ขณะนี้ คือ พวก nucleoside analog ได้แก่ Azidothymidine (AZT) หรือ Zidovudine, dideoxyionosine (ddI), dideoxycytidine (ddC) และที่ยังอยู่ในระหว่างการประเมินผลอีกหลายขนานอาทิ 3' Deoxy thymidine- 2' ene หรือ d4T ส่วนพวก non-nucleoside analog ได้แก่ tetrahydroimidazol benzodiazepin (TIBO), Foscarnet ซึ่งมีฤทธิ์ยับยั้งไวรัสกลุ่มเชื้อเริม และ Cytomegalovirus, Dipyridodiazepinone (B1 -RG -587) ซึ่งทั้งหมดยังอยู่ในระหว่างการประเมินผล
๑.๒ สารยับยั้งมิให้เชื้อไวรัสเข้าสู่เซลล์ยังอยู่ในขั้นการประเมินผลได้แก่ soluble CD4 โมเลกุล, dextran sulfate และ Carbomethoxy carbonyl-pyrolyl-phenalamine esters (CPFs)
๑.๓ สารยับยั้งเอนไซม์โปรติเนส (Proteinase inhibitor) ซึ่งจะทำให้อนุภาคไวรัสใหม่ที่ได้ไม่สมบูรณ์ ยาที่กำลังประเมินผลในกลุ่มนี้ ได้แก่ Castanospermine และ 1 - deoxy-nojirimycin (N - butyl - DNJ) ปัจจุบันนี้ได้เริ่มนำมาใช้แล้ว
๑.๔ สารยับยั้งการถอดและแปลรหัสบนยีนของเชื้อเอชไอวี ได้แก่ Ribozyme, antisense molecules และการทำ gene therapy ทั้งหมดยังอยู่ในขั้นการพัฒนาและวิจัย
๒.๑ อินเตอร์เฟอรอน
๒.๒ อินเตอร์ลิวคิน-๒, อินเตอร์ลิวคิน -๑๐
๒.๓ อิมูไธออล หรือ DTC ๒.๔ อิมเร็ก -๑ เป็นต้น
ได้มีรายงานการใช้ยา AZT ในมารดาติดเชื้อเอชไอวีที่ตั้งครรภ์ว่า ได้ผลดีในการป้องกันการแพร่เชื้อจากมารดาไปสู่ทารกขณะนี้ได้เริ่มใช้กันในบางประเทศแล้ว
วัคซีนป้องกันการติดเชื้อเอชไอวีได้มีการพัฒนาและประเมินผลมาเป็นเวลาเกือบ ๑๐ ปี ในแง่ความปลอดภัยและการกระตุ้นให้เกิดภูมิคุ้มกันทั้งแบบเซลล์และแอนบอดี มีวัคซีนหลายชนิด ที่ทำการประเมินผลในคนกลุ่มเล็กไปแล้วให้ผลดีทั้งในแง่ความปลอดภัยและการกระตุ้นภูมิคุ้มกันในผู้ได้รับวัคซีน แต่ยังไม่มีการประเมินผลของวัคซีนเหล่านี้ในกลุ่มประชากรกลุ่มใหญ่ที่มีอัตราเสี่ยงต่อการติดเชื้อเอชไอวีสูงจึงยังไม่ทราบว่าวัคซีนเหล่านี้จะได้ผลในการป้องกันการติดเชื้อหรือไม่
วัคซีนการป้องกันการติดเชื้อเอชไอวี ที่ดีควรมีคุณสมบัติ ดังนี้
๑) ก่อให้เกิดแอนติบอดีชนิดลบล้างฤทธิ์ไวรัส (neutralizing) ที่สามารถป้องกันการติดเชื้อเอชไอวีได้ทุกสายพันธุ์ที่ระบาดในโลก
๒) ก่อให้เกิดภูมิคุ้มกันทั้งแบบเซลล์และแอนติบอดีตอบสนองต่อเซลล์ติดเชื้อเอชไอวี
๓) ก่อให้เกิดภูมิคุ้มกันที่สามารถกำจัดเซลล์ที่มีเชื้อเอชไอวีแอบแฝง
๔) ไม่กระตุ้นให้เกิดแอนติบอดีชนิดเอนฮานซิง (enhancing) ที่กลับจะทำให้มีการติดเชื้อเอชไอวีเพิ่มขึ้นอย่างรวดเร็ว
๕) ไม่ก่อให้เกิดภูมิคุ้มกันชนิดที่ทำลายเซลล์ของตัวเอง (autoimmune response)
๖) ก่อให้เกิดภูมิคุ้มกันเฉพาะที่ (local immunity) ตรงตำแหน่งที่เชื้อเอชไอวีเข้าสู่ร่างกายเป็นทางเข้าของเชื้อเอชไอวี
๗) ปลอดภัย
๘) ภูมิคุ้มกันที่เกิดอยู่ได้นาน
วัคซีนที่ได้รับการพัฒนาขึ้น เพื่อป้องกันการติดเชื้อเอชไอวีและได้มีการทดสอบระยะที่ ๑ และ ๒ ในอาสาสมัครทีติดเชื้อและไม่ติดเชื้อเอชไอวี ได้แก่
๑. โปรตีนส่วน envelope (rgp160) ที่ถูกผลิตโดยวิธีพันธุวิศวกรรม ใช้ไวรัสเอชไอวี -๑ (HIV-1)
๒. Vaccinia virus ที่มียีน envelope ของเอชไอวีอยู่เป็น recombinant virus ใช้ไวรัสสายพันธุ์แอลเอวี (LAV)
๓. การใช้ rgp 160 และ vaccinia recombinant env HIV-1 ร่วมกันในการทดสอบในอาสาสมัครที่ไม่ติดเชื้อเอชไอวี
๔. โปรตีน envelop (gp 120) ผลิตโดยวิธีพันธุวิศวกรรมจากเซลล์ของยีสต์ใช้ไวรัสสายพันธุ์เอสเอฟ ๒ (SF2)
๕. โปรตีน envelope ส่วน gp 120 ผลิตโดยวิธีพันธุวิศวกรรมในเซลล์ของ Chinese hamster ovary ใช้ไวรัสสายพันธุ์เอสเอฟ ๒ (SF2)
๖. โปรตีน envelope ส่วน gp 160 ผลิตโดยวิธีพันธุวิศวกรรมจาก Vero cells โดยใช้ Vaccinia virus เป็นพาหะนำยีน vector ใช้ไวรัสสายพันธุ์ IIIB
๗. โปรตีน envelope ส่วน gp 120 ผลิตโดยวิธีพันธุวิศวกรรมจากเซลล์ของ Chinese hamster ovary ใช้ไวรัสสายพันธุ์ IIIB, MN และ
๘. โปรตีนสังเคราะห์ ส่วน p17 (HGP- 30) ใช้ไวรัสสายพันธุ์ IIIB
๙. อนุภาคที่คล้ายไวรัสและมีแอนติเจน p 24 (Ty-p24 virus like particle) ใช้ไวรัสสายพันธุ์ IIIB
๑๐. Vaccinia virus ที่มียีนของ envelope (gp 160) ใช้ฉีดครั้งแรกและฉีดกระตุ้นด้วยโปรตีนสังเคราะห์ ไวรัสสายพันธุ์ที่ใช้คือ IIIB
๑๑. โปรตีน gp160 ผลิตโดยวิธีพันธุ- วิศวกรรม จากเซลล์ BHK-21ใช้ฉีดครั้งแรกและกระตุ้นด้วยโปรตีนสังเคราะห์ ส่วน V3 ใช้ไวรัสสายพันธุ์ MN/BRU
๑๒. Canarypox virus ที่มียีน gp 160 ของไวรัสสายพันธุ์ MN/BRU อยู่ ใช้ฉีดครั้งแรกและกระตุ้นด้วยโปรตีน gp 160 จากไวรัสสายพันธุ์ MN/BRU ที่ผลิตในเซลล์ BHK-21
๑๓. เซลล์เม็ดเลือดขาวของอาสาสมัครที่ติดเชื้อ vaccina virus ที่มียีน gp160 สายพันธุ์ IIIB อยู่ ใช้ฉีดครั้งแรกและกระตุ้นด้วยแอนติเจนของเอชไอวี (HIV-๑)
๑๔. ไวรัสเอชไอวีที่ไม่มียีนสำหรับส่วน gp 120 ถูกทำให้หมดฤทธิ์ด้วย B-propriolactone และ Co-60 ใช้ไวรัสสายพันธุ์ H2-321
๑๕. โปรตีนสังเคราะห์ส่วน V3 ของ gp120 ที่เป็นจำนวน ๘ โมเลกุล (octameric) โดยการเชื่อมของกรดอะมิโน lysine มีทั้งที่ใช้ไวรัสสายพันธุ์ MN (monovalent) และแบบที่มีสายพันธุ์อื่น ๆ (multivalent) ผสมกัน
ประเทศไทยได้รับคัดเลือกให้เป็น ๑ ใน ๔ ประเทศทั่วโลกที่จะได้ทดลองวัคซีนป้องกันเอชไอวี โดยการสนับสนุนขององค์การอนามัยโลกขณะนี้วัคซีนที่ได้มาทดลองในคนไทย ได้แก่ วัคซีนของบริษัท UBI และ Genentech ซึ่งตรงกับชนิดของวัคซีนในข้อที่ ๗ และ ๑๕
