เมื่อนำโลหะ Mg มาทำปฏิกิริยากับสารละลายกรดไฮโดรคลอริก (HCl) เกิดปฏิกิริยาดังสมการ
Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g)
ต่อมาได้ทำการปรับเปลี่ยนการทดลองเพิ่มเติม 2 ครั้ง ดังนี้
ครั้งที่ 1 เปลี่ยนโลหะที่ใช้เป็น Al ที่มีมวลเท่าเดิม และใช้กรด HCl ที่มีความเข้มข้นเท่าเดิม พบว่าการเกิดแก๊สไฮโดรเจนช้าลง
ครั้งที่ 2 เปลี่ยนชนิดของกรดเป็นกรดซัลฟิวริก (H2SO4) ที่มีความเข้มข้นเท่าเดิม และใช้โลหะ Mg ที่มีมวลเท่าเดิม พบว่าการเกิดแก๊สไฮโดรเจนไวขึ้น
ถ้าทำการทดลองเพื่อหาอัตราการเกิดแก๊สไฮโดรเจน 6 การทดลอง โดยแต่ละการทดลองใช้โลหะที่มีมวลเท่ากัน มีข้อมูลการทดลองดังตาราง
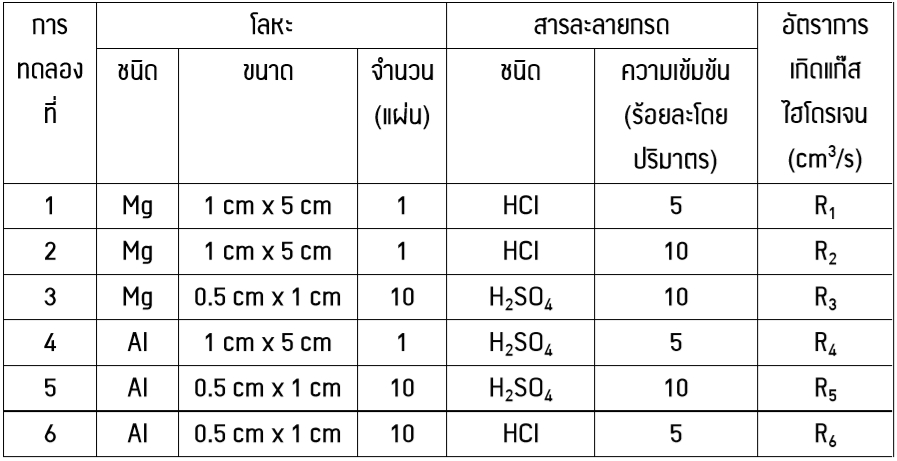
จากผลการทดลอง การเปรียบเทียบอัตราการเกิดแก๊สไฮโดรเจนในข้อใดไม่ถูกต้อง
ตอบ 3) R5 > R3
ข้อที่ 1 ถูก เพราะ ใช้โลหะ Mg ที่มีลักษณะเหมือนกัน ใช้กรด HCl เหมือนกัน แต่การทดลองที่ 2 กรดมีความเข้มข้นมากกว่าการทดลองที่ 1 จึงทำให้ R2 > R1
ข้อที่ 2 ถูก เพราะ ถึงแม้ว่าทั้งสองการทดลองใช้โลหะ Mg เหมือนกัน แต่ในการทดลองที่ 3 โลหะ Mg มีพื้นที่ผิวเกิดปฏิกิริยามากกว่าการทดลองที่ 2 และถึงแม้จะใช้กรดที่มีความเข้มข้นเท่ากัน แต่การทดลองที่ 3 ใช้กรดที่มีความว่องไวต่อการเกิดปฏิกิริยามากกว่าการทดลองที่ 2 จึงทำให้ R3 > R2
ข้อที่ 3 ผิด เพราะ ถึงแม้ว่าจะใช้กรดชนิดเดียวกัน ความเข้มข้นของสารละลายกรดเท่ากัน และใช้โลหะที่มีพื้นที่ผิวเกิดปฏิกิริยาเท่ากัน แต่การทดลองที่ 5 ใช้โลหะ Al ซึ่งมีความว่องไวในการเกิดปฏิกิริยาน้อยกว่าโลหะ Mg จึงทำให้ R5 < R3
ข้อที่ 4 ถูก เพราะ ถึงแม้ว่าทั้งสองการทดลองใช้โลหะ Al และใช้สารละลายกรด H2SO4 เหมือนกัน แต่ในการทดลองที่ 5 โลหะ Al มีพื้นที่ผิวเกิดปฏิกิริยามากกว่า และสารละลายกรดมีความเข้มข้นมากกว่า ทำให้ R5 > R4
ข้อที่ 5 ถูก เพราะ ถึงแม้ว่าใช้โลหะ Al ที่มีพื้นที่ผิวเกิดปฏิกิริยาเท่ากัน แต่การทดลองที่ 5 ใช้กรดที่มีความว่องไวในการเกิดปฏิกิริยามากกว่า และมีความเข้มข้นมากกว่า จึงทำให้ R5 > R6







