พิจารณาการทดลอง 3 การทดลองเพื่อศึกษาอัตราการเกิดปฏิกิริยาเคมีระหว่างสารละลายกรดไฮโดรคลอริก (HCl) กับเปลือกไข่ (มีส่วนประกอบหลักคือ CaCO3) ซึ่งมีปฏิกิริยาเคมีเกิดขึ้นดังสมการ
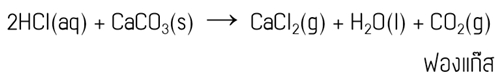
พิจารณาการทดลองต่อไปนี้
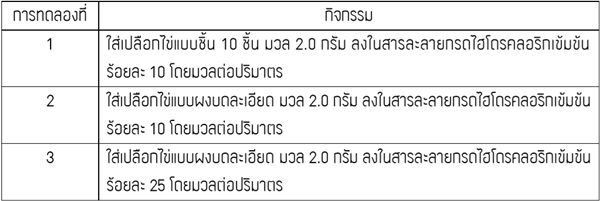
หากนักเรียนทำการทดลองแล้วเปรียบเทียบอัตราการเกิดปฏิกิริยาเคมี โดยการวัดปริมาตรแก๊สที่เกิดขึ้น ผลการทดลองควรเป็นอย่างไร
คำตอบ ข้อ 4) อัตราการเกิดปฏิกิริยาในการทดลองที่ 3 มากกว่าการทดลองที่ 1
หากเปรียบเทียบข้อแตกต่างระหว่างการทดลองทั้ง 3 ในด้านต่อไปนี้
- ลักษณะของสารตั้งต้น (เปลือกไข่) ในทั้ง 3 การทดลองใช้เปลือกไข่ปริมาณเท่ากัน แต่การทำผงเปลือกไข่บดละเอียดจะเป็นการช่วยเพิ่มพื้นที่ผิวสัมผัสในการเกิดปฏิกิริยาเคมี ดังนั้นเปลือกไข่แบบบดละเอียดจะทำให้มีอัตราการเกิดปฏิกิริยาที่เร็วกว่าเปลือกไข่แบบเป็นชิ้น
- ความเข้มข้นของกรดที่ใช้ นอกจากเปลือกไข่ที่มีส่วนประกอบเป็น CaCO3 แล้ว ยังมีกรดซึ่งเป็นสารตั้งต้นอีกชนิดหนึ่งของปฏิกิริยา กรดที่เข้มข้นมากกว่าจะทำให้มีอัตราการเกิดปฏิกิริยาที่เร็วกว่ากรดที่เข้มข้นน้อยกว่า
ดังนั้น หากเรียงลำดับอัตราการเกิดปฏิกิริยาเคมีจากน้อยไปมากจะได้ว่า 1 < 2 < 3
* เมื่อปฏิกิริยาเกิดขึ้นจนสิ้นสุด ไม่มีแก๊สเกิดขึ้นอีกต่อไป เมื่อวัดปริมาตรแก๊สที่เกิดขึ้นในแต่ละการทดลองจะได้เท่ากัน เนื่องจากมวลของเปลือกไข่ทั้ง 3 การทดลองมีจำกัดที่ 2.0 กรัม เท่ากัน ไม่ว่าจะมีปริมาณกรดมากเพียงใด ดังนั้น หาก CaCO3 ที่อยู่ในเปลือกไข่เกิดปฏิกิริยาจนหมดแล้ว ปฏิกิริยาเคมีก็จะหยุดชะงักลง
ไม่สามารถเกิดแก๊สเพิ่มเติมได้อีก








